Quetiapine bij Parkinson-psychose: zinvol of zinloos?
Critical Appraisal of a Topic

Anne Vievermans, Daisy Janssen
Klinische situatie
Een 89-jarige patiënte met de ziekte van Parkinson (ZvP) en hypertensie ervaart steeds vaker visuele hallucinaties met lijdensdruk. Zo ziet ze een kind dat in brand staat en haar overleden partner. Haar medicatie wordt volgens voorschrift ingenomen, er zijn geen recente wijzigingen hierin geweest en in overleg met de neuroloog wordt de dosering levodopa/cardidopa gehandhaafd. Na analyse lijken de hallucinaties te passen bij psychotische symptomen bij ZvP. Clozapine, de eerste medicamenteuze keus bij psychotische symptomen bij de ZvP,1 heeft niet de voorkeur van mevrouw vanwege het vereiste bloedprikken. Quetiapine wordt als tweede medicamenteuze keus overwogen, maar twijfels bestaan over de effectiviteit.2
Klinische vraag
Wat is het effect van quetiapine (I) op de verbetering van psychotische symptomen (O), bij een oudere patiënte met de ZvP zonder cognitieve stoornis (P), in vergelijking met placebo? (C)
Zoekstrategie
Er werd gezocht op 01-03-2025 in PubMed met de volgende zoektermen: ((((((((parkinson's disease[MeSH Terms]) OR (parkinson disease)) OR (parkinson's disease)) OR (parkinson)) AND (((((disorder, psychotic[MeSH Terms]) OR (psychosis)) OR (psychotic)) OR (psychotic symptoms)) OR (hallucinations))) AND ((Quetiapine) OR (Seroquel))) AND ((((controlled clinical trials, randomized[MeSH Terms]) OR (RCT)) OR (Randomized controlled trial)) OR (Randomised controlled trial))) AND (((placebo effect[MeSH Terms]) OR (placebo)) OR (placebos))) AND ((((Effect) OR (symptom relief)) OR (improvement)) OR (quality of life)).
Zestien artikelen werden gevonden waarvan zes niet geschikt leken voor de klinische vraag. Redenen hiervoor waren: een andere interventie (1 artikel), quetiapine bij een ander ziektebeeld dan ZvP (4 artikelen), andere interventie en ziektebeeld (1 artikel). Tien artikelen waren mogelijk wel geschikt, bestaande uit vier Randomized Controlled Trials (RCT’s) en zes reviews. Deze RCT’s kwamen terug in de reviews. De systematische review van Desmarais et al. (2016)3 werd gekozen omdat deze specifiek keek naar quetiapine bij psychotische symptomen in de ZVP.
Overzicht uitkomsten
De gekozen review kijkt naar het effect van quetiapine op psychotische symptomen, in vergelijking met placebo of clozapine bij mensen met de ZVP; Lewy Body Dementie (LBD) of andere neurodegeneratieve aandoening met parkinsonisme. De uitkomstmaat met betrekking tot psychotische symptomen wordt in de meeste RCT’s beschreven middels de “Brief Psychiatric Rating Scale (BPRS)” ,4 naast nog enkele andere (minder gebruikte) psychiatrische schalen (NPI, CGIS). De BPRS is een klinisch instrument waarmee 18 psychiatrische symptomen, waaronder hallucinaties, wanen en angst, op een schaal van 1 (afwezig) tot 7 (zeer ernstig) worden beoordeeld; hogere totaalscores weerspiegelen ernstigere psychopathologie. Een secundaire uitkomstmaat is motorische bijwerkingen; uitgedrukt als de Unified Parkinsons’s Disease Rating Scale (UPDRS).5 Er is voor deze secundaire uitkomstmaat gekozen omdat verergering van motorische symptomen een veelvoorkomend en klinisch relevant risico is bij het gebruik van antipsychotica bij de ZvP. Er werden 7 studies met 241 deelnemers geïncludeerd, waarvan 2 keken naar quetiapine vs. clozapine en 5 keken naar quetiapine vs. placebo. Vanwege de vraag wordt gefocust op laatstgenoemde. Al deze 5 studies werden dubbelblind verricht. In 4 van de 5 studies was dementie geen exclusiecriterium. Alleen in de studie van Ondo et al. (2005)6 werd dementie wél uitgesloten, waardoor deze studie het best aansloot bij de onderzoeksvraag. De auteurs van deze studie rapporteerden echter geen kwantitatieve resultaten van de gebruikte schalen (BPRS en UPDRS), waardoor de resultaten niet in de tabel met gemiddelde scoreveranderingen konden worden opgenomen.
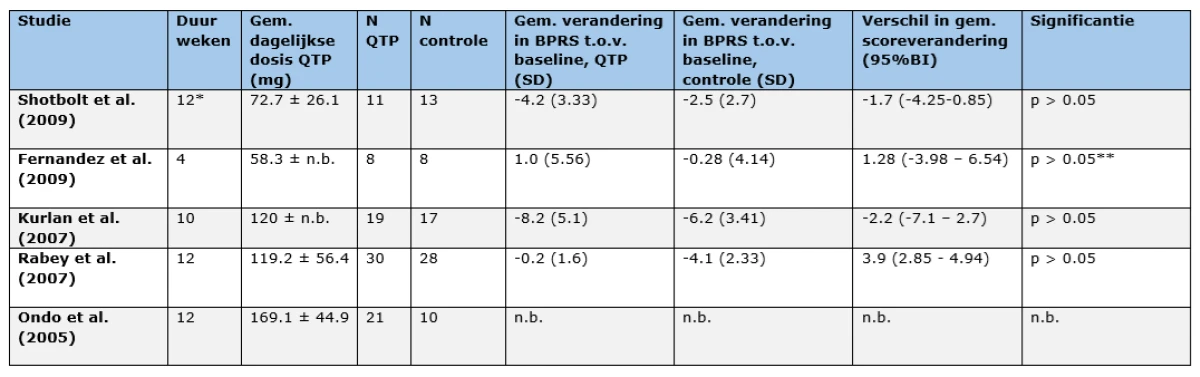
Van alle geïncludeerde patiënten was 57% man, met een gemiddelde leeftijd van 72 jaar. Van de 241 geïncludeerde patiënten was er 32.4% uitval (reden onbekend). Er was geen statisch significante daling in de BPRS-scores bij quetiapine of placebo, t.o.v. baseline. Het verschil in de gemiddelde scoreverandering (quetiapine vs. placebo) varieerde tussen de -2.2-+3.9. Alleen de studie van Fernandez et al. (2009; n=16)7 rapporteerde een significant voordeel van quetiapine ten opzichte van placebo op het BPRS-item hallucinaties. De studies van Ondo et al. (2005) [6] en Rabey et al. (2007)8 vonden geen significant verschil op dit item (hoewel dit in de review niet expliciet wordt uitgelicht). De overige studies rapporteerden uitsluitend totaalscores op de BPRS, zonder uitsplitsing naar afzonderlijke items (Tabel 1). In geen van de studies werd een significante verslechtering van motorische symptomen gevonden; de gemiddelde UPDRS-scores bleven stabiel. Van de 122 patiënten die quetiapine kregen, rapporteerden 10 een toename van parkinsonisme, waarvan 4 enkel subjectief gerapporteerd en 6 objectief vastgesteld (door onderzoekers als mild beoordeeld). Niet-motorische bijwerkingen werden niet gerapporteerd.
Tabel 1. Belangrijkste uitkomstmaten quetiapine v.s. placebo (controle)
Evaluatie
Deze systematische review wordt op basis van de AMSTAR-2-criteria9 ingeschat als van matige kwaliteit. Sterke punten zijn de onderzoeksvraag met uitgebreide literatuursearch in meerdere databases, selectie van artikelen, data-extractie in duplicaat en beoordeling met de Cochrane Risk of Bias-tool.10 Het artikel rapporteert duidelijke resultaten en houdt rekening met beperkingen van de geïncludeerde studies. Er zijn echter ook kritische tekortkomingen, waaronder het ontbreken van een vooraf geregistreerd protocol, geen duidelijke motivatie voor het uitsluitend includeren van RCT’s en het ontbreken van een volledige lijst met uitgesloten studies. Dit beperkt de transparantie en vergroot het risico op selectiebias. Daarnaast was dementie geen exclusiecriterium, hetgeen zowel de respons op medicatie als de betrouwbaarheid van symptoommetingen kan beïnvloeden. Daarbij ontbraken gedetailleerde gegevens uit de enige studie waarin dementie wél als exclusiecriterium gold (Ondo et al. (2005).6] Dit beperkt de mogelijkheid om valide conclusies te trekken over het effect van quetiapine bij patiënten met de ZvP zonder cognitieve stoornissen. De kleine hoeveelheid studies en de hoge heterogeniteit maakten een meta-analyse onmogelijk, waardoor gepoolde effectschattingen ontbreken en de nauwkeurigheid en generaliseerbaarheid beperkt zijn. Het hoge uitvalspercentage (32,4%), waarvan de redenen niet zijn gerapporteerd, kan de resultaten vertekenen. In combinatie met het ontbreken van systematische rapportage van andere bijwerkingen blijft het veiligheidsprofiel onvolledig en bestaat het risico dat de verdraagbaarheid van quetiapine te gunstig wordt ingeschat. De review laat zien dat quetiapine (gemiddeld 100 mg/dag) in de onderzochte RCT’s geen significante verbetering van psychotische symptomen opleverde vergeleken met placebo. Deze lagere dosering werd bewust gekozen vanwege de kwetsbaarheid van de oudere populatie en om mogelijke motorische bijwerkingen te beperken. De auteurs benoemen dat deze doseringen lager zijn dan de gebruikelijke doseringen bij schizofrenie waardoor het mogelijk onvoldoende krachtig was om psychotische symptomen te verminderen.11 Omdat geen duidelijke dosis-responsrelatie werd gevonden, blijft het echter onzeker of hogere doseringen wel tot meer effect zouden leiden. Gezien deze tekortkomingen moeten de resultaten kritisch worden geïnterpreteerd. Er blijft behoefte aan een grootschalige, goed gecontroleerde RCT met strikte definities van de patiëntpopulatie om de effectiviteit van quetiapine te onderzoeken.
Gevolg voor de casus
De resultaten, die met inachtneming van de beperkingen van het onderzoek moeten worden geïnterpreteerd, zijn tevens niet geheel toepasbaar op de patiënt uit de casus. Het merendeel in de studie is man en jonger dan onze patiënte. De setting is niet vergelijkbaar: de studies werden niet verricht in een verpleeghuis en ook niet in Nederland. Dementie was geen exclusiecriterium in de meeste onderzoeken en andere comorbiditeiten worden niet beschreven. Ondanks het beperkte en zwakke bewijs voor effectiviteit van quetiapine op psychotische symptomen vanuit deze studie, kan een proefbehandeling met quetiapine in deze casus worden overwogen vanwege de veiligheid ten aanzien van motorische symptomen, het ontbreken van beter geaccepteerde alternatieven en de klinische noodzaak om de lijdensdruk te verminderen. Daarbij moet rekening worden gehouden met mogelijke andere bijwerkingen die in de huidige studies niet systematisch zijn beschreven, zodat zorgvuldige monitoring essentieel blijft. De patiënte in onze casus startte met quetiapine 1dd12,5 mg wat later werd opgehoogd naar 2dd 12,5 mg. Zij had minder last van haar hallucinaties en ervoer geen bijwerkingen.
Auteurs
Drs. Anne Vievermans, aios ouderengeneeskunde, Maastricht University
Prof. dr. Daisy J.A. Janssen, hoogleraar ouderengeneeskunde, Maastricht University
Literatuur
Bloem BR, Van Laar T, Keus SHJ, De Beer H, Poot E, Buskens E, et al. Multidisciplinaire richtlijn Ziekte van Parkinson (namens de Centrale Werkgroep Multidisciplinaire richtlijn Parkinson 2006–2010). Alphen aan den Rijn: Van Zuiden Communications; 2010 [geraadpleegd op 4 maart 2025]. Beschikbaar via: https://www.parkinsonnet.nl/app/uploads/2019/11/multidisciplin_rl_parkinson_final_version.pdf
Richtlijnendatabase. Ziekte van Parkinson [internet]. [z.d.] [geraadpleegd op 4 maart 2025]. Beschikbaar via: https://richtlijnendatabase.nl/richtlijn/ziekte_van_parkinson/startpagina_ziekte_van_parkinson.html
Desmarais P, Massoud F, Filion J, Nguyen QD, Bajsarowicz P. Quetiapine for psychosis in Parkinson disease and neurodegenerative Parkinsonian disorders: a systematic review. J Geriatr Psychiatry Neurol. 2016;29(4):227–236. https://doi.org/10.1177/0891988716640378
Overall JE, Gorham DR. The Brief Psychiatric Rating Scale. Psychol Rep. 1962;10:790–812 [geraadpleegd op 4 maart 2025]. Beschikbaar via: https://www.statpower.net/Content/312/Homework/OverallGorham1962.pdf
Martínez-Martín P, Gil-Nagel A, Gracia LM, Gómez JB, Martínez-Sarriés J, Bermejo F. Unified Parkinson's Disease Rating Scale characteristics and structure. Mov Disord. 1994;9(1):76–83. https://doi.org/10.1002/mds.870090112
Ondo, W. G., Tintner, R., Voung, K. D., Lai, D., & Ringholz, G. (2005). Double-blind, placebo-controlled, unforced titration parallel trial of quetiapine for dopaminergic-induced hallucinations in Parkinson’s disease. Movement Disorders, 20(8), 958–963. https://doi.org/10.1002/mds.20410
Fernandez HH, Okun MS, Rodriguez RL, Malaty IA, Romrell J, Sun A, et al. Quetiapine improves visual hallucinations in Parkinson disease but not through normalization of sleep architecture: results from a double-blind clinical-polysomnography study. Int J Neurosci. 2009;119(12):2196–2205. https://doi.org/10.3109/00207450903222758
Rabey, J. M., Prokhorov, T., Miniovitz, A., Dobronevsky, E., & Klein, C. (2007). Effect of quetiapine in psychotic Parkinson’s disease patients: A double-blind labeled study of 3 months’ duration. Movement Disorders, 22(3), 313–318. https://doi.org/10.1002/mds.21251
Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J, et al. AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ. 2017;358:j4008. https://doi.org/10.1136/bmj.j4008
Higgins JP, Altman DG, Gøtzsche PC, et al. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ. 2011;343:d5928. https://doi.org/10.1136/bmj.d5928
Arvanitis, L. A., & Miller, B. G. (1997). Multiple fixed doses of “Seroquel” (quetiapine) in patients with acute exacerbation of schizophrenia: A comparison with haloperidol and placebo. Biological Psychiatry, 42(4), 233–246. https://doi.org/10.1016/S0006-3223(97)00225-4